Schéma De Lewis
- Heure Australie Melbourne
- un-seul-deviendra-invincible-5
- Schéma du cycle menstruel de la femme
- Schéma de Lewis , exercice de Chimie - 236114
- Schéma de lewis du propane
- Schéma de Lewis
Électrons de valence Rappel Le cortège électronique d'un atome est constitué de couches, correspondant à des niveaux d'énergie croissante. Plus la couche sur laquelle se trouve un électron est à un niveau élevé, moins celui-ci est lié au noyau. Définition Électrons de valence: Les électrons de valence d'un atome constituent la couche externe de son cortège électronique. Ces électrons sont les moins liés au noyau. En fonction de la place d'un élément dans le tableau périodique, on peut déterminer le nombre d'électrons de valence qu'il possède, et le niveau auquel ils se trouvent. Le tableau ci-dessous présente le nombre d'électrons de valence (entre parenthèses) des atomes des éléments des trois premières lignes du tableau périodique. La première colonne indique la couche de valence ( 1 1, 2 2 ou 3 3).
Schéma du cycle menstruel de la femme

Les atomes perdent ou gagnent des électrons afin de se transformer en un ion monoatomique stable. Le schéma de Lewis permet de rendre compte de la stabilité de structures telles que les ions monoatomiques. Les électrons se répartissent selon des couches électroniques, caractérisées par des nombres entiers n, et des sous-couches, caractérisées par des lettres. La dernière couche avec des électrons est la couche électronique de valence ou couche externe. Un atome perd ou gagne des électrons de sa couche de valence afin d'acquérir la structure électronique du gaz noble le plus proche dans la classification périodique: il se transforme en ion monoatomique stable. Sur la couche de valence, les électrons sont groupés par paquets de deux: les doublets électroniques non liants. mot clé Une lacune électronique correspond à deux électrons en moins par rapport à la règle du duet et de l'octet. Dans un schéma de Lewis, on représente les doublets électroniques non liants par des tirets autour du symbole de l'atome et les lacunes électroniques par des rectangles.
Schéma de Lewis , exercice de Chimie - 236114
Activit�: Titrage de la B�tadine (TP 12): PDF Exercice: Titrage � d'une eau de javel: Titrage de l'eau oxyg�n�e: PDF Titrage du Fer III par l'�tain: PDF Exercice; Titrage de l'acide oxalique: PDF Titrage du dioxyde de soufre dans le vin: PDF Titrage du diiode par le thiosulfate: PDF Semaine 13: ���������������� Mouvement et interactions 1. Interactions fondamentales et introduction � la notion de champ. Interaction �lectrostatique et champ �lectrique (TP 13): PDF Semaine 14: ���������������� Activit�: Deux interactions fondamentales (TP 14): PDF Exp�rience de Millikan: PDF Trou noir: PDF Semaine 15: 2. Description d�un fluide au repos. Activit�: Forces pressante: PDF Activit�: Loi de la statique des fluides (TP 15): PDF Semaine 16: Activit�: Loi de Mariotte (TP 16): PDF Constitution et transformations de la mati�re 2. De la structure des entit�s aux propri�t�s physiques de la mati�re. A) De la structure � la polarit� d�une entit�. Semaine 17: Activit� 1: Sch�ma de Lewis: PDF Activit� 2: Electron�gativit� et polarisation des liaisons: PDF Activit�: Sch�ma de Lewis - g�om�trie des mol�cules (TP 17): PDF M�thodologie mol�cules: PDF D�terminer la nature des atomes et leur g�om�trie: PDF B) De la structure des entit�s � la coh�sion et � la solubilit�/miscibilit� d�esp�ces chimiques.
- Offre black et decker
- Schéma de la communication
- Schéma de lewis de l'ion
- Schéma de lewis and clark
- Formation et schéma de Lewis d’un ion monoatomique | Annabac
- Schéma de lewis de n2o
- Schéma de la dent à compléter
Retour Sommaire - Revoir la leçon 7 PROBLEME AVEC CORRIGE n° 7- A: Structure des atomes, molécules et ions. Question 1: Corriger éventuellement les affirmations suivantes: La représentation de Lewis d'une molécule ou d'un ion polyatomique permet de mettre en évidence: a- la répartition des électrons externes. ( c) b- la manière dont les atomes sont liés entre eux. ( c) c- la disposition, dans l'espace à trois dimensions, des atomes. ( c) Réponse: a- ( e) oui, on représente les électrons de la dernière couche. b- ( e) oui c- ( e) non Question 2: a- Donner la formule électronique et la structure de Lewis des atomes suivants: 1 H 6 C 7 N 8 O 9 F 15 P 16 S 17 Cl b- Donner la structure de Lewis des molécules ou ions suivants: NH 3 H 2 O H 3 O + HO - CH 3 Cl C 2 H 6 C 2 H 4 HF H 2 S CH 3 CH 2 OH CH 3 CHO HCO 3 - a- ( e) Donnons la formule électronique et la structure de Lewis des atomes suivants: b- ( e) Donnons la structure de Lewis des molécules ou ions demandés. On précisera même la géométrie (hors programme cette année) en appliquant la méthode VSEPR ( voir la leçon 7).
Schéma de lewis du propane
Dans les ions polyatomiques, il est courant d'indiquer quel atome porte la charge. La charge négative de l'ion hydroxyde HO − \text{HO}^- est portée par l'atome d'oxygène, qui attire plus facilement les électrons que les atomes d'hydrogène. Pour la même raison, la charge positive de l'ion hydronium H 3 O + \text{H}_3 \text{O}^+ est plus probablement répartie entre les atomes d'hydrogène: la représentation de Lewis localise cette charge sur un des trois atomes sans préférence particulière. La molécule de trichlorure d'aluminium est une substance très réactive utilisée comme catalyseur dans des procédés industriels. Ceci est dû à la lacune électronique de l'atome d'aluminium, dont la couche de valence ne présente que 6 6 électrons. Astuce Il est commode de représenter d'abord les atomes constitutifs d'une molécule, pour repérer les doublets non liants et les liaisons covalentes à former. Géométrie des molécules Les doublets non liants d'un atome et les liaisons covalentes dans lesquelles un atome est impliqué sont répartis de manière à minimiser les interactions répulsives entre ces paires d'électrons.

Note: La règle du duet ne concerne que l'hydrogène, l'hélium et le lithium en vue d'avoir une configuration proche de celle de l'hélium. On dit aussi que l'objectif des atomes est d'être le plus stable possible de façon à avoir une structure électronique externe la plus proche possible du gaz rare (ou gaz noble) le plus proche. Ces gaz sont dans la dernière colonne du tableau périodique de Mendeleïev. Détermination du nombre de liaisons A partir du numéro atomique d'un atome, on connait le nombre d'électrons qu'il possède (numéro atomique = nombre de protons = nombre d'électrons). A partir de ce nombre d'électrons, on détermine le nombre d'électrons pour chaque couche électronique. On détermine ensuite le nombre d'électrons célibataires sur la couche de valence (la plus externe). Enfin, on détermine le nombre de liaisons possibles en soustrayant le nombre d'électrons célibataires au nombre maximal d'électrons que peut accueillir la couche de valence. Exemple de l'oxygène: 8 – 6 = 2 liaisons.
Schéma de Lewis
Exemples Atome de carbone Atome d'hydrogène Atome d'oxygène Atome d'azote L'un des intérêts de la formule de Lewis est de permettre de prévoir la géométrie des molécules. En effet, cette dernière obéit à un principe relativement simple: tous les doublets ( liants et non liants, simples ou multiples) se répartissent dans l'espace de manière à être éloignés au maximum les uns des autres en raison de la forces électriques répulsives qui s'exercent entre eux. Il est ainsi possible d'associer à chaque répartition de doublets autour d'un atome une géométrie (tétraédrique, pyramidale, plane etc) Les formules de Lewis présentent un intérêt particulier pour expliquer la réactivité chimique de certaines espèces et pour décrire les « mécanismes réactionnels» (les étapes intermédiaires d'une transformation chimique). En effet, les doublets liants correspondent à des zones de « concentration électronique » susceptibles de manifester une affinité pour les zones de « déficit électronique » ce qui permet d'expliquer la formation ou la rupture de liaisons entre certain groupements lors de la description d'un mécanisme réactionnel.
Déterminer le schéma de Lewis d'un ion monoatomique Voici les noms et les numéros atomiques associés à plusieurs atomes: lithium Li ( Z = 3); azote N ( Z = 7); sodium Na ( Z = 11); magnésium Mg ( Z = 12) a. Déterminer pour chaque atome, la structure électronique. b. Déterminer le nombre d'électrons perdus ou gagnés par chacun des atomes pour former l'ion. c. Déterminer le schéma de Lewis de chacun des ions monoatomiques formés. conseils a. Rappelez-vous que les sous-couches électroniques se remplissent dans l'ordre suivant: 1s; 2s; 2p; 3s; 3p. Une sous couche s peut contenir au maximum deux électrons et une sous couche p, six au maximum. Le numéro atomique est égal au nombre d'électrons que possède l'atome. b. Appliquez la règle de stabilité d'un atome qui tend à perdre ou à gagner des électrons. c. Si l'atome perd des électrons, il donne un cation (positif) tandis que s'il en gagne, il devient un anion (négatif). Les électrons de la couche externe se regroupent en doublets non liants qui sont représentés par des traits placés à côté du symbole de l'atome.
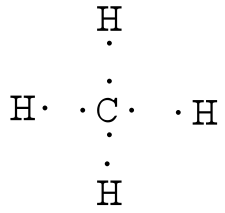
Schéma de Lewis Les électrons interviennent dans la représentation de Lewis d'une molécule. Pour bien comprendre cette représentation il faut tout d'abord savoir ce qu'est une liaison covalente; c'est la mise en commun de deux électrons externes. Deux électrons externes forment un doublet liant. La liaison covalente peut également être simple, double ou triple. Prenons comme exemple la molécule de méthane. Sa formule est CH 4 Il faut calculer le nombre d'électrons externes de chaque atome. L'atome de carbone (C) possède 6 protons donc 6 électrons car un atome est toujours électriquement neutre. Cortège électronique du carbone: (K)² (L) 4 y a donc 4 électrons externes. Nous allons faire de même pour l'hydrogène (H). possède 1 proton donc 1 électron car un atome est toujours électriquement neutre. électronique de l'hydrogène: (K) 1 possède donc 1 électron externe. Ensuite, il fut calculer le nombre total d'électrons externes: 4+4*1=8 y a donc en tout 8 électrons externes ( il faut multiplier le nombre d'électrons externes de chaque élément: ici l'hydrogène est représenté par H 4 donc 1 électron externe*4=4).
La liaison covalente Afin de former des molécules, plusieurs atomes sont liés par des liaisons covalentes. Cette liaison consiste en un partage d'électrons entre deux atomes. Une liaison covalente est représentée par un trait. On parle également de doublet liant. Il peut également y avoir des liaisons doubles entre deux atomes, représentées par deux traits. La dernière possibilité est d'avoir des liaisons triples, représentées par trois traits. On parle de liaisons covalentes multiples. Les liaisons triples sont les plus stables car il est logiquement plus difficile de casser trois liaisons qu'une seule ou même deux. En parallèle, certains électrons dits libres ne sont engagés dans aucune liaison. On les appelle aussi électrons célibataires. Lorsque deux électrons célibataires sont appariés (forment une paire), on parle de doublet non liant. Schématisation de la transformation de deux atomes d'oxygène en une molécule de dioxygène et visualisation selon le modèle de Lewis Note: Seuls les électrons de la couche électronique la plus externe peuvent former des liaisons.